快速且清晰的類器官三維影像分析
使用 Nikon ECLIPSE Ji 全自動細胞影像擷取系統,搭配 AI 與去卷積影像處理技術
近年來,人工智慧(AI)與影像處理技術的突破,讓使用者能以簡單操作快速取得高品質的 3D 影像。雖然螢光顯微鏡(epi-fluorescence microscopy)具備在短時間內獲取大量影像的優勢,但由於樣品較厚時會出現模糊的非焦距面螢光訊號,導致對比度下降。透過 3D 去卷積(3D deconvolution)運算可以有效降低這些模糊光,顯著提升影像品質。此外,延伸景深功能(Extended Depth of Focus, EDF)能將 3D 資料合成聚焦清晰、高對比的 2D 影像。本文將介紹如何應用 AI 與影像處理技術,快速取得類器官(organoids)的 3D 影像。
▶ 高效整合螢光與共軛焦成像的工作流程 ▶ Experiment 1:利用 3D 去卷積與 EDF 進行螢光成像 ▶ Experiment 2:採用高倍數物鏡與 2D 去卷積進行螢光成像 ▶ Experiment 3:使用高倍數矽油物鏡進行共軛焦成像 ▶ AI 優勢
▶ 了解更多 Nikon ECLIPSE Ji 全自動細胞影像擷取系統

(3D 去卷積與延伸景深,EDF)
(B) (C) 螢光標記 E-cadherin(Alexa Fluor 594)的腸類器官(三維小腸上皮細胞培養系統)影像,(B) 為 3D 去卷積前,(C) 為 3D 去卷積後。由於 (B) 中存在離焦光,導致對比度降低;而 (C) 中模糊光被有效去除,
E-cadherin 的網狀結構得以清晰呈現。
(D) 將經過 3D 去卷積的 39 層 Z-stack 影像合成為單張延伸景深(EDF)影像,並合併顯示細胞核(藍色:DAPI)與 E-cadherin(橘色:Alexa Fluor 594)螢光通道。
(E) 為 (D) 中紅框區域的放大圖。
(F) 為 (E) 中分離出來的 E-cadherin 螢光通道影像。
比例尺:100 μm (D)、25 μm (E) (F) 。
【影像擷取條件】
• 成像方式:螢光(Epi-fluorescence)
• 物鏡:PLAN APO λD 20x(數值孔徑 NA 0.8)
• Z-stack:每層 0.8 μm,共 39 層(Z 軸總範圍:30.40 μm)
高效整合螢光與共軛焦成像的工作流程
Autosignal.ai 是一套利用 AI 技術自動判斷樣品最適曝光條件的系統,只需一鍵即可完成影像設定。使用螢光顯微鏡可快速找出感興趣區域,再切換至共軛焦顯微鏡,即可獲得解析度更高的 3D 影像,有助於深入理解樣品的三維結構。

Experiment 1:利用 3D 去卷積與 EDF 進行螢光成像
本實驗在 18 秒內使用兩種螢光波長取得 39 層 Z-stack 影像。從「樣品導覽」(Sample Navigation)功能獲取整片玻片影像、精準定位樣品、取得約 30 μm 厚度的類器官影像、直至影像處理完成,整體流程僅約 3 分 30 秒。這種快速的成像流程,能有效提升類器官樣品的高通量影像獲取效率與清晰度。
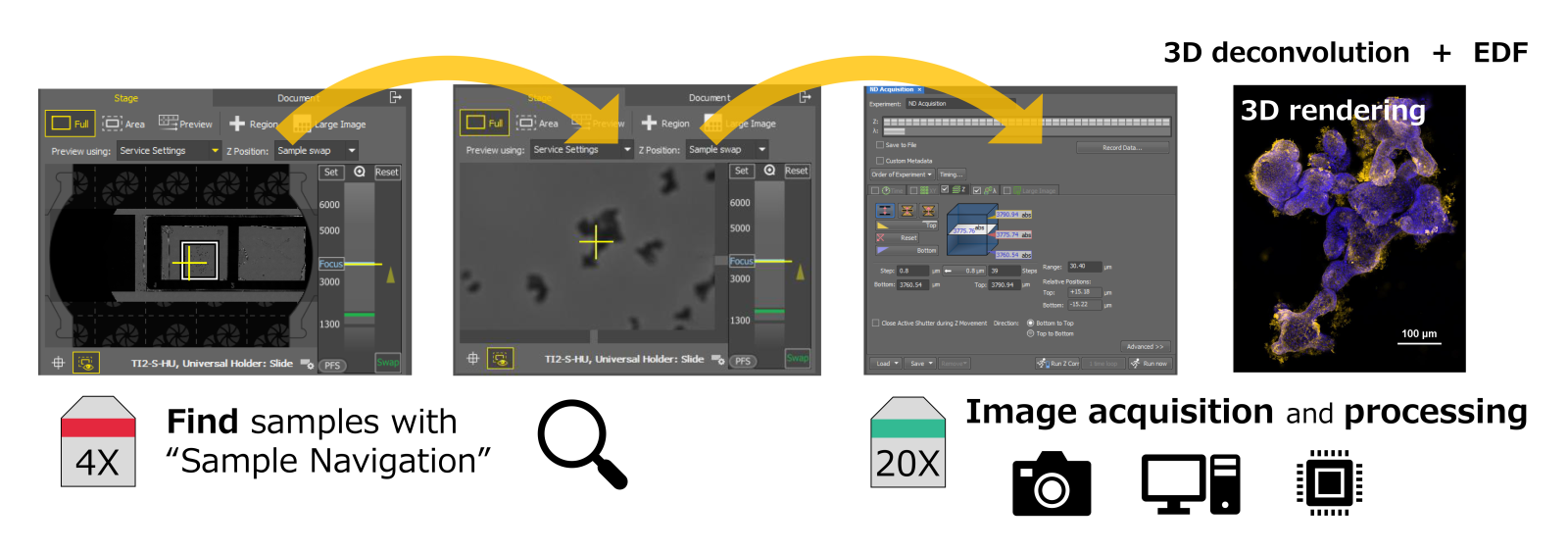
Step 1:「Sample Navigation」功能可拍攝整張玻片範圍,協助快速定位樣本位置。
Step 2:先使用 4X 物鏡尋找目標類器官,再切換至 20X 物鏡,透過「ND Acquisition」功能擷取 Z-stack 影像。
Step 3:對 Z-stack 影像進行 3D 去卷積處理以減少模糊光,接著利用 EDF(延伸景深)功能建立單張全聚焦影像。
這是一套適用於類器官成像與高解析三維影像分析的 AI 自動化工作流程。
影像擷取與處理總耗時:共 1 分 38 秒
• 影像擷取時間:18 秒(放大倍率:20X,Z-stack:每層 0.8 μm × 39 層,Z 軸範圍:30.40 μm)
• 影像處理時間:1 分 20 秒(使用 Richardson-Lucy 演算法進行 3D 去卷積:52 秒,EDF(延伸景深)處理:28 秒)
*處理平台:NVIDIA Quadro RTX 4500 GPU
Experiment 2:採用高倍數物鏡與 2D 去卷積進行螢光成像
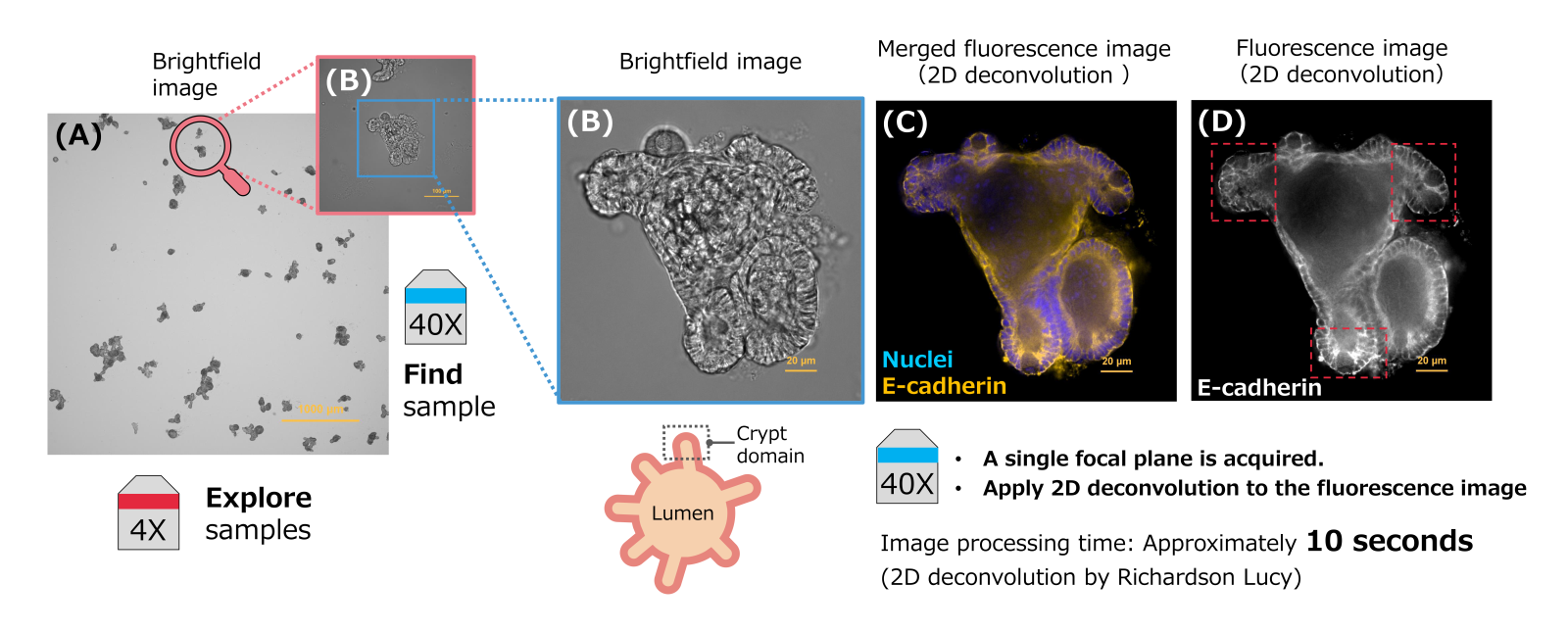
圖2:使用螢光成像與 2D 去卷積技術觀察帶有 crypt domains 的腸類器官(enteroids)
(B) 帶有 crypt domains 的腸類器官明視野影像,物鏡:PLAN APO λD 40x(NA 0.95)。
(C) 經 2D 去卷積處理後的多色螢光疊圖影像(細胞核:藍色,DAPI;E-cadherin:橘色,Alexa Fluor 594)。
(D) 來自影像 (C) 的 E-cadherin 單通道螢光影像。使用高數值孔徑的 PLAN APO λD 40x(NA 0.95)物鏡所拍攝的影像具有較淺的焦深,因此只能觀察樣品體積中較薄的一層。對此影像進行 2D 去卷積處理後,可更清晰地觀察 crypt domains (詳見 D 圖中紅色虛線框處)。
比例尺:1000 μm (A),20 μm (B) (C) (D) 。
Experiment 3:使用高倍數矽油物鏡進行共軛焦成像
在未經組織透明化處理的腸道類器官深層區域中,光線容易被吸收,影像亮度下降。Denoise.ai 是一套以 AI 為基礎的影像降噪功能,能利用已訓練好的神經網絡模型,從共振掃描共軛焦影像中去除 shot noise(散粒噪聲),以提升影像品質。當將 Denoise.ai 應用於高速共振掃描器所取得的影像時,不僅成功移除了雜訊,甚至在黑暗、深層區域也能大幅改善影像品質(詳見圖3,D1、D2),讓我們得以清晰觀察 crypt domains 中 Paneth 細胞周圍的結構。
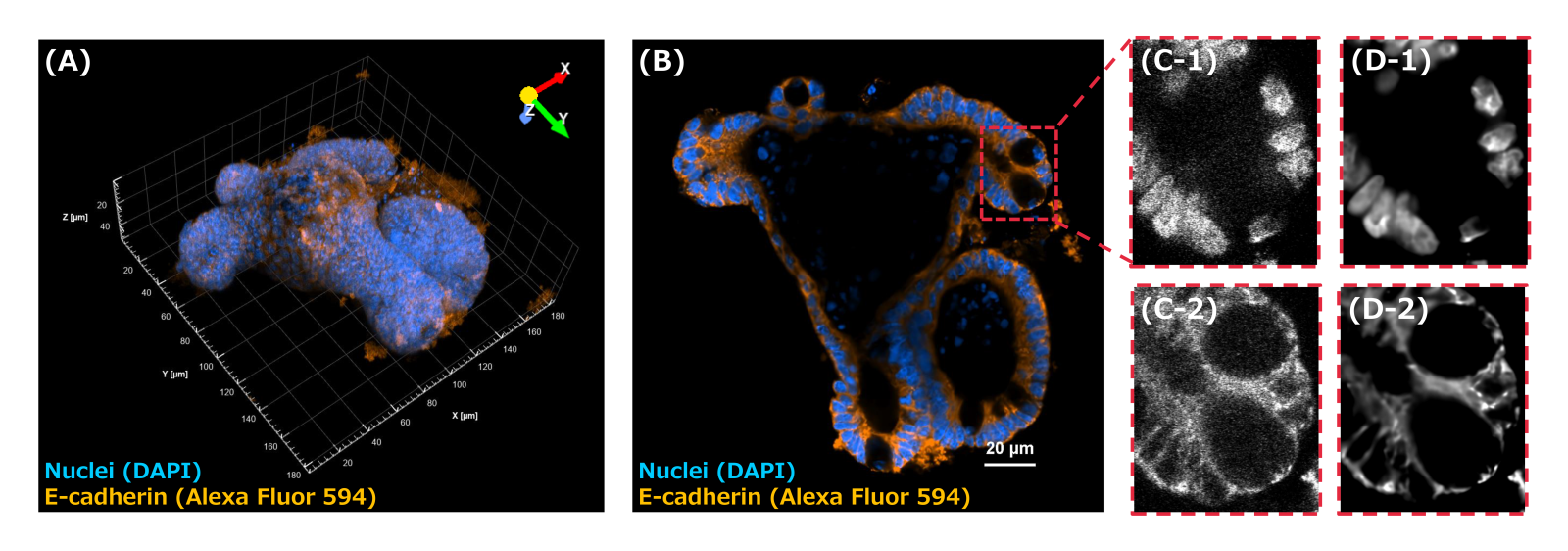
圖3:使用 Denoise.ai 提升含 crypt domains 的腸類器官共軛焦影像成像品質
比例尺:20 μm(B)
(A) 腸類器官的三維體積重建影像,由 227 張影像組成(Z軸範圍:53.30 μm)。
(B) 在 Z=123 處的光學切片影像(Z深度:28.77 μm)。
(C) (D) B圖中紅色虛線框選區域的放大影像。
(C1, C2) 應用 Denoise.ai 前的原始影像。
(D1, D2) 應用 Denoise.ai 後的處理影像。
(C1, D1) 細胞核(DAPI)的共軛焦影像。
(C2, D2) E-cadherin(Alexa Fluor 594)的共軛焦影像。
【影像擷取條件】
• 物鏡:Plan Apo Lambda S 60XC 矽油浸物鏡(NA 1.3)
• 縮放倍率:1.3x
• 掃描方式:共振式掃描器
• 影像解析度:2K x 2K 像素
• 平均取樣:4 次
• Z 軸範圍:53.30 μm(Z-stack:每層 0.236 μm,共 227 層)
AI 優勢
1. 操作簡便:自動化影像擷取與處理流程,使取得清晰影像變得更容易。
2. 結合影像處理技術的螢光顯微鏡優勢
• 快速影像擷取:透過影像系統進行拍攝,以高幀率取得影像,能迅速識別感興趣區域。
• 去除模糊光以提升影像品質:2D / 3D 去卷積技術可移除非焦距面螢光訊號,提供細節更銳利的影像。
3. 共軛焦顯微鏡與影像處理的優勢
• 取得 3D 影像:可於三度空間影像中進行光學切片觀察,幫助深入理解三維結構。
• 適用於厚樣品:共軛焦顯微鏡能有效去除離焦光,提供高解析度且清晰的影像。
• 降噪處理:Denoise.ai 能去除 shot noise,改善快速掃描或低亮度樣品的成像品質。
4. 結合螢光與共軛焦影像的優勢
高效率識別感興趣區域:可快速擷取螢光成像影像,快速辨識目標區域,再利用共軛焦顯微鏡擷取 3D 影像並觀察細節。整合這兩種成像方式,有助於縮短從區域篩選到精細觀察的整體流程時間,提升研究效率。
